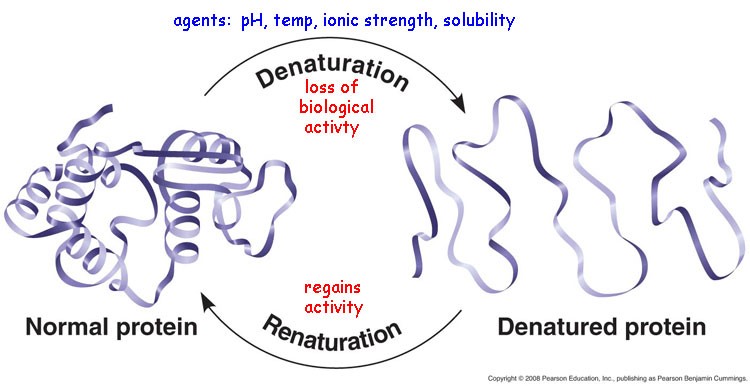
蛋白質(zhì)因受某些物理或化學因素的影響,分子的空間構(gòu)象被破壞���,從而導致其理化性質(zhì)發(fā)生改變并失去原有的生物學活性的現(xiàn)象稱為蛋白質(zhì)的變性作用(denaturation)�。變性作用并不引起蛋白質(zhì)一級結(jié)構(gòu)的破壞���,而是二級結(jié)構(gòu)及以上的高級結(jié)構(gòu)的破壞��,變性后的蛋白質(zhì)稱為變性蛋白���。
在變性條件不劇烈�����,變性蛋白質(zhì)內(nèi)部結(jié)構(gòu)變化不大時��,除去變性因素�,在適當條件下變性蛋白質(zhì)可恢復其天然構(gòu)象和生物活性����,這種現(xiàn)象稱為蛋白質(zhì)的復性(renaturation)。
但在實際研究中發(fā)現(xiàn)�����,在體外折疊時�,蛋白質(zhì)分子間由于存在大量錯誤折疊和聚合,復性效率往往很低�����。究其原因���,蛋白質(zhì)的立體結(jié)構(gòu)雖然由其氨基酸順序決定�,然而伸展肽鏈折疊為天然活性結(jié)構(gòu)的過程還受到周圍環(huán)境的影響。蛋白質(zhì)復性實驗是一個復雜的過程�。
基本流程
從破碎細胞開始,然后將細胞勻漿離心�����,回收包涵體后���,加入變性劑溶解包涵體,使之成為可溶性伸展態(tài)���,再通過透析等除去變性劑使表達產(chǎn)物折疊恢復天然構(gòu)象及活性��。
考慮到不同蛋白質(zhì)包涵體的特定結(jié)構(gòu)與理化特性�����,采用不同的變性變復性方法�����。復性條件包括pH��、溫度����、蛋白濃度、離子濃度等����。復性輔助劑包括分子伴侶、氧化還原對等��。獲得高品質(zhì)可溶活性蛋白��。
(資料來源:百度百科�����、第八章基因工程下游技術(shù))

 南京-德泰生物
南京-德泰生物 南京-金斯瑞
南京-金斯瑞 北京-英茂盛業(yè)生物
北京-英茂盛業(yè)生物